ニュース
2018年07月30日
心血管腎臓病に克つために
- キーワード
- 糖尿病の検査(HbA1c 他) 糖尿病合併症
血圧変動が腎機能低下と動脈硬化進展のリスク因子
まず一つ目の柱である血圧に関連し、この領域の最近のトピックと言えば2017年のAHA(American Heart Association)/ACC(American College of Cardiology)で発表された米国の新たな高血圧診断基準だろう。つい最近まで血圧管理を緩める傾向にあったものが、 SPRINT試験(Systolic Blood Pressure Intervention Trial)の結果を受けて突然のように厳格化され、従来prehypertensionとされていた130~139/80~89mmHgもステージ1の高血圧と定義された1)。
しかし、SPRINTにおいてベースライン時にCKDを有していた群のサブグループ解析をみると、厳格降圧群と通常降圧群とで主要評価項目である心血管イベントと腎イベントのいずれも有意差がない。ところが全死亡に関しては厳格降圧群で有意に抑制されていた2)。この点が重視された結果、前述の診断基準改訂につながったのであろう。しかしCKD患者の予後には人種差があり、日本人では死亡よりも末期腎不全リスクの方が高いとの報告がある3~6)。また最近では日本人のネフロン数は欧米人の3分の2ほどしかなく、生来的に腎臓が弱い可能性も指摘されている7)。よって海外のエビデンスの解釈は慎重であらねばならず、わが国発のエビデンスが求められる。
そこで我々がいま注目しているのが先ほど述べた血圧変動だ。既報ではCKDのステージ進行とともに血圧変動パターンがnon-dipper、riserを呈する患者が増え8)、それに伴い心血管疾患発症リスクが有意に増加することが示されているが9)、我々は血圧変動へ介入することによる臓器障害への影響を検討している。現在までに、診察室血圧の低下幅よりもABPM(Ambulatory Blood Pressure Monitoring)で把握した夜間睡眠時血圧の それの方が、腎障害のマーカーであるアルブミン尿の改善とより強く相関することを明らかにしている10)。また病態連関の視点から動脈硬化にも目を向けbaPWV(brachial-ankle Pulse Wave Velocity)との相関も検討したが、同様の結果が得られている。
正脂血症のASO患者にもLDLアフェレーシスが有効
研究の二つ目の柱は、血清脂質正常のASO発症透析患者に対するLDLアフェレーシスだ。先進医療Bとして厚労省から認可され全国唯一の施設として行っており、循環器科と腎臓内科を一体化した我々の教室の特色を生かした取り組みと言える。
これまでの成果として、治療抵抗性ASO患者の歩行可能距離がLDLアフェレーシスによって有意に改善すること11, 12)、eNOS(endothelial Nitric Oxide Synthase)活性化が歩行可能距離やABI(Ankle Brachial pressure Index)の改善と有意に相関すること13,14)などを報告してきた。LDLアフェレーシスの効果は単にLDL-Cを低下させるだけでなく、酸化ストレスや炎症系、凝固系を抑制するなどの経路を介して内皮機能を向上させ、その結果ASOの症状改善に結び付くと考えている。
長寿遺伝子Sirtuin1との関連からも注目されるATRAP
三つ目の柱の基礎的研究ではAT1の下流に位置する情報伝達系の研究を進めている。主要なターゲットは我々がATRAP(angiotensin II receptor associated protein)と呼ぶ、AT1受容体C末端に特異的に結合する蛋白質だ。
ATRAPは、AT1受容体が刺激を受け細胞内にinternalization(内在化)する過程を促進することで受容体機能を選択的に阻害すると考えられている。まだ研究途上ではあるが、現在までにわかったポイントを述べてみたい。
ATRAPは腎尿細管上皮に多く発現しており、腎機能低下や寿命とも関連を認める
ATRAPを高発現させたトランスジェニックマウスも通常飼育下では、野生型マウスと血圧や心機能・形態に何ら変わりない。ところが心肥大刺激を加えて飼育すると、野生型マウスではp38-MAPK(Mitogen-Activated Protein Kinase)が活性化し心肥大が進行する一方、ATRAP高発現マウスはその変化を認めない15~17)。つまり、病的刺激が存在する時にATRAPは臓器保護的に働く可能性がある。
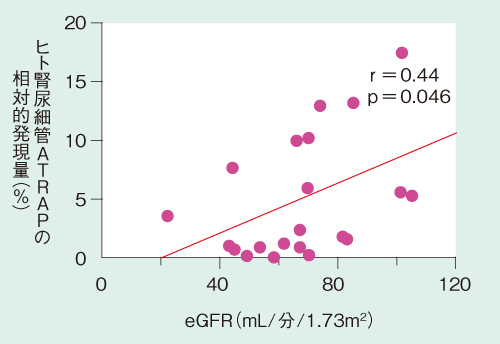
このATRAPの発現は2型糖尿病モデルマウスでは有意に低下しており、ヒトにおいても糖尿病やMet-S(Metabolic Syndrome)で発現が低下している18)。そしてヒト生体内でのATRAPの組織分布をみると、脂肪組織や心血管系、筋肉などにもみられるが、最も多く発現しているのは腎尿細管、ことに上皮細胞であることがわかった19)。またヒトにおいて腎尿細管のATRAPの発現はeGFRが低いほど減少することも示され(図2)、腎機能の低下に伴ってATRAPの機能も低下してくると考えられる。
この他、ATRAPをノックアウトした5/6腎摘マウスでは、野生型マウスに比べて血圧が有意に上昇しナトリウム再吸収チャネルの発現が増加することを報告しており20)、腎組織の線維化が亢進することも確認した。またこれらの違いの背景として長寿遺伝子と呼ばれるSirtuin1の腎臓における発現がATRAPノックアウトマウスで低下していることも見出している。
我々の検討ではATRAPノックアウトマウスは寿命が18.4%短縮しており、これをヒトに当てはめると15~17年に相当する。最近『NHKスペシャル』で「腎臓が寿命を決める」と放送され話題になったが、仮にそうだとすると腎尿細管でのATRAPの発現もそれに関与しているのかもしれない。
糖尿病の検査(HbA1c 他)の関連記事
- 針を刺さない血糖測定への挑戦―「超音波」で血糖の状態を知る新技術
- 糖尿病の人の熱中症を防ぐための10ヵ条 猛暑は血糖管理を悪化させる? 十分な対策を
- 減塩食が糖尿病の合併症リスクを低下 塩分を減らすと血圧を下げられる 【おいしく減塩する方法】
- 糖尿病と肥満のある人が体重を減らすとお得がいっぱい たとえ減量に失敗してもメリットが 食事日記をつければ成功率は2倍に
- 肥満のある人が体重を減らすと糖尿病リスクは大幅減少 中年期の体重管理は効果が高い 血糖値を下げる薬を止められる人も
- 糖尿病の合併症を防ぐために「高血糖」と「高血圧」の治療が必要 高血圧があるとリスクは3倍に上昇
- 【笑いが糖尿病を改善】 お笑いライブ鑑賞でストレスが減り楽観性が向上 「笑いヨガ」の効果
- 糖尿病の人は歯を失いやすい 血糖管理が良好だと歯も丈夫に 糖尿病の治療と歯科受診が大切
- 腎臓病は糖尿病の人が発症しやすい合併症 腎臓病の治療は進歩している 透析にならないために
- 糖尿病と高血圧があると腎臓病リスクが上昇 運動時間をわずか5分増やすだけで血圧は低下【高血圧の日】

 医療・健康情報グループ検索
医療・健康情報グループ検索