ニュース
2016年09月09日
食事に応じた脂肪合成の遺伝子スイッチの仕組みを解明 治療へ前進

空腹時に肝臓での脂肪の合成を抑制し、食後に促進する遺伝子のスイッチ切り替えの仕組みが明らかになった。食事状況に応じて肝臓での中性脂肪の合成がオン・オフされる仕組みがはじめて解明された。
研究を発表したのは、筑波大学医学医療系の矢作直也准教授、武内謙憲助教らの研究グループ(筑波大学医学医療系ニュートリゲノミクスリサーチグループ)。
食事による遺伝子のスイッチをオン・オフする仕組みを解明
細胞の中の遺伝子の発現は、転写因子と呼ばれる遺伝子によって制御されている。「KLF15」は、脂肪細胞の分化に関わり、肥満状態の発現をコントロールするタンパク質。
研究チームは、「KLF15」が脂肪の合成に関与し、その発現を増強させると、血中の中性脂肪値が低下し、脂質異常症が改善することを突き止めた。
食事から過剰に摂取された炭水化物は、体内合成によってエネルギー貯蔵物質である中性脂肪に変えられ、脂肪組織などに蓄えられる。過食に伴い体内の中性脂肪が過剰になる状態が肥満で、糖尿病・高血圧・脂質異常症を併発しやすくなる。
これらは動脈硬化の危険因子でもあり、中性脂肪の合成・蓄積をコントロールする治療が求められている。
炭水化物から中性脂肪への合成・変換は食後に増加し、空腹時に減少する。この経路が食事状況に応じてどのように調節されているのかは不明だった。
そこで研究チームは、肥満のモデルマウスを使った実験で、肝臓で「KLF15」の発現を増強させると、血中の中性脂肪値が低下することを明らかにした。
in vivo(生体内)イメージング装置を用い、食事の摂取状況によって中性脂肪を合成する経路を制御する遺伝子「SREBP-1」を生きたマウスの肝臓内で可視化した。
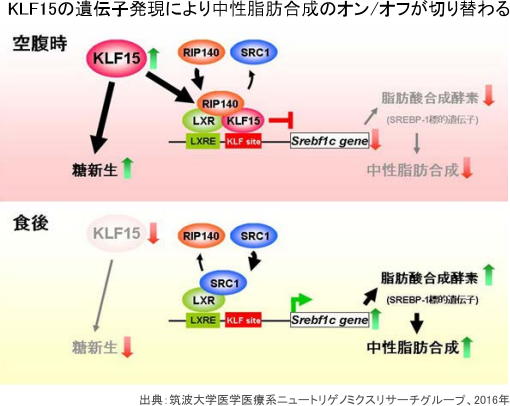
絶食時には肝臓の核内でSREBP-1のプロモーター(遺伝子発現に関与する領域)に「KLF15」を含むタンパク質複合体が形成され、この複合体が転写抑制因子を呼びこみ、SREBP-1の転写をオフにすることを突き止めた。これにより、絶食時には中性脂肪の合成が抑制されることが分かった。
一方、摂食後には同複合体から「KLF15」がなくなり、転写抑制因子が転写促進因子と入れ替わり、SREBP-1の転写をオンにすることが明らかになった。これにより、摂食後には中性脂肪合成が促進されるという。
また、肥満のマウスでは肝臓の「KLF15」の発現が低下しており、これを増加させると肥満マウスの高脂血症が改善することも判明した。治療的観点からも「KLF15」の重要性が明らかになった。
今回の研究は、2型糖尿病や肥満、脂質異常症の治療法の開発につながる可能性がある。成果は米科学誌「セル・リポーツ」電子版に発表された。
(代表者: 筑波大学医学医療系・准教授 矢作直也)
独自開発の新技術基盤によるニュートリゲノミクスの探求から代謝疾患の病態解明を目指し研究している。
[ Terahata ]
日本医療・健康情報研究所
医療の進歩の関連記事
- 最新版!『血糖記録アプリ早見表2026-2027』を公開
- 遠隔医療で妊娠糖尿病妊婦の離島出産を支援、小豆島で第1例が誕生
- 息で糖尿病を検出するセンサーが開発進行中
- 先進医療技術の普及により1型糖尿病患者の血糖管理が大きく改善
- 注射だけでない未来へ「飲むインスリン」研究のいま
- 糖尿病の治療薬メトホルミンが長寿に関係 老化を遅らせ寿命を延ばす薬に期待
- 【1型糖尿病の最新情報】幹細胞から分化した膵島細胞を移植 インスリンが不要になり重症低血糖もゼロに
- 【1型糖尿病の最新情報】発症からインスリン枯渇までの期間を予測 より効果的な治療を期待 日本初の1型糖尿病研究
- 「異種移植」による腎臓移植が最長記録 米国で臨床試験の開始を公表
- 最新版!『血糖記録アプリ早見表2025-2026』を公開
