ニュース
2020年05月07日
1型糖尿病の発症を腸内細菌が抑制 腸内環境が自己免疫疾患に大きく関わっている

自己免疫疾患である1型糖尿病の発症に、白血球(T細胞)の働きが大きく関わっており、腸内に生息するある種の線虫や細菌がその免疫機能を抑制していることが、理化学研究所の研究で明らかになった。
「自己免疫疾患が増加したのは感染症が減少したからだ」という「衛生仮説」を科学的に証明したもので、1型糖尿病の新たな予防・治療法の開発につながると期待されている。
「自己免疫疾患が増加したのは感染症が減少したからだ」という「衛生仮説」を科学的に証明したもので、1型糖尿病の新たな予防・治療法の開発につながると期待されている。
1型糖尿病の予防・治療に新たな光
自己免疫疾患とは、本来は外来から侵入してくる異物から生体を守るはずの免疫システムが異常をきたして、誤って自分自身の細胞や組織を攻撃してしまう疾患。
1型糖尿病は、インスリンを分泌する膵臓のβ細胞が自分の免疫細胞によって破壊され、そこから分泌されるインスリンが絶対的に不足し、高血糖が引き起こされる自己免疫疾患だ。欧米では患者が増加していることが報告されている。
これに対して2型糖尿病は、肥満などが原因で、インスリンが分泌されていても十分に効かなくなるインスリン抵抗性を要因として発症する疾患で、1型糖尿病とは原因がまったく異なる。2型糖尿病は生活習慣が要因だが、1型糖尿病は生活習慣と関係なく発症する。
環境が衛生的になり自己免疫疾患が増えた?
衛生が改善し清潔な環境が増えた影響で、過去に比べて寄生虫病や結核などの感染症が減少している。一方で、アレルギーや自己免疫疾患などは増加しており現代病とされている。
乳幼児期の衛生環境は免疫系の発達に影響を及ぼしており、自己免疫疾患などが増加したのは感染症が減少したためではないかと考えられており、「衛生仮説」と呼ばれている。
自己免疫疾患などの患者が増加している背景には、衛生環境の改善や生活水準の向上、予防接種の普及、食生活・栄養の変化、抗生物質の乱用による幼少時の感染症の減少が関与していることが多くの疫学調査で分かってきた。
たとえば、薬剤の普及により寄生虫の感染者数が劇的に減少した地域では、自己免疫疾患の患者数が増加することが疫学的に明らかにされている。
寄生虫に感染すると、宿主(ヒト、マウスなど)は免疫機能を発達させ、寄生虫を体外へ排出しようとする。これに対して、寄生虫は宿主の免疫機能を低下させるシステムをもつため、宿主の攻撃を回避できると考えられている。
したがって、寄生虫による感染症を予防・治療するために、このシステムの解明が重要であり、寄生虫が誘導する(免疫抑制性の)細胞の種類や分泌する物質を同定する研究が世界中で行われている。
腸管にいる線虫が1型糖尿病の発症を抑制
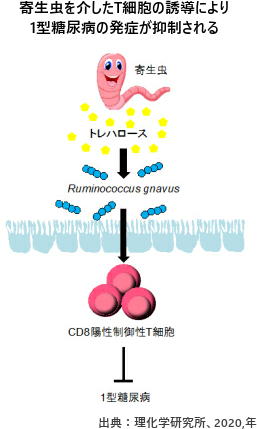
線虫が分泌する糖が腸内細菌を増やしT細胞を誘導
研究グループは次に、H. polygyrusがどのようにCD8Tregを誘導するのかを調べた。H. polygyrusは、主に小腸上部(十二指腸)に寄生する寄生虫なので、感染したマウスの小腸にある代謝産物を解析した。
すると、感染マウスでは腸管内で「トレハロース」という糖が増加しており、H. polygyrus自身がこれを分泌していることが分かった。さらに、トレハロースは腸内細菌の餌になっていることが分かった。
トレハロースは二糖類の一種で、耐糖能改善や、神経変性疾患の抑制、細胞の保護など、さまざまな生理機能があることが知られており、食品や化粧品、飼料などの原料にも使用されている。
次世代シーケンサーを使い腸内細菌叢の変化を解析したところ、H. polygyrusがトレハロースを分泌することで別の腸内細菌が増殖し、この腸内細菌によってT細胞であるCD8Tregが誘導され、その結果、膵臓のβ細胞の破壊がくいとめられ、1型糖尿病の発症を抑えられることが明らかになった。
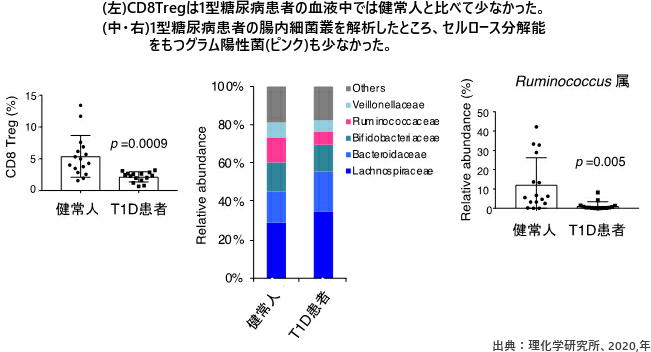
さらに、1型糖尿病患者の血液を調べたところ、CD8Tregが減少しており、これを誘導する腸内細菌が少ないことも分かった。
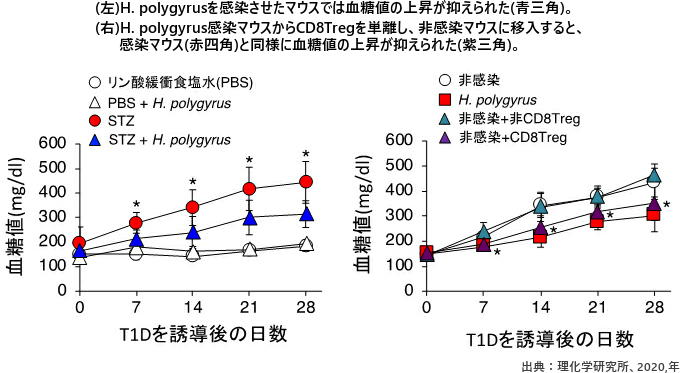
線虫や腸内細菌がT細胞を誘導 1型糖尿病を抑制
これまでにも、CD8Tregは多発性硬化症や全身性エリテマトーデスなどの自己免疫疾患に効果があることが動物実験で示されている。
今回の研究で、CD8Tregを誘導し1型糖尿病の発症を抑制するために、寄生虫が分泌するトレハロースと、それによって増殖した腸内細菌が必要であることが明らかになった。
1型糖尿病を根治する治療法は見つかっていない。膵移植や膵島移植といった治療は選択肢の1つになるが、ドナー不足などの課題があり、実施数は伸び悩んでいる。
1型糖尿病患者は、現時点ではインスリンを頻回注射やインスリンポンプで補う治療を一生涯にわたり続ける必要があり、これが患者に大きな負担を強いている。
「今後、このCD8Tregの誘導メカニズムや膵臓での抑制メカニズムを明らかにすることで、1型糖尿病の新たな予防・治療法を開発できる可能性がある」と、研究グループは述べている。
研究は、理化学研究所生命医科学研究センター粘膜システム研究チームの下川周子客員研究員(国立感染症研究所寄生動物部主任研究官、群馬大学大学院医学系研究科生体防御学協力研究員)と大野博司チームリーダー、国立感染症研究所寄生動物部の久枝一部長らの共同研究グループによるもの。研究成果は、「Nature Communications」に掲載された。
CD8+ regulatory T cells play a critical role in prevention of autoimmune-mediated diabetes", Nature Communications(Nature Communications 2020年4月22日)
[ Terahata ]
日本医療・健康情報研究所
1型糖尿病の関連記事
- 「患者さんとその家族のための 糖尿病治療の手びき2026」3年ぶりの改訂版発売 日本糖尿病学会
- 東京都が1型糖尿病の妊婦さんを支援 インスリンポンプ等の費用助成を開始
- 厚生労働省が糖尿病の普及啓発資材を公開 リーフレット・動画の2形態
- 1型と2型のどちらの糖尿病も認知症リスクを高める
- 「楽しい」気持ちが行動を後押し 漫画による子どもの糖尿病教育の効果
- 発足から24年、「国際糖尿病支援基金」がウェブサイトをリニューアル
- インスリン治療を50年以上続けてきた人を称える「インスリン50年賞」を15名に授与
- 11月14日は世界糖尿病デー 2025年は「糖尿病と職場」に焦点をあて、働く人が安心して過ごせる社会の実現へ
- 医療用テープで肌トラブルを起こさないための対策とは
- 不安を笑顔に変える場所 YOKOHAMA VOXがホームページをリニューアル

